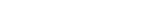GMAのこれまでとこれから:GMAのクリニカルパール探求

アダカラムインタビュー記事シリーズ
GMA 20年をこえる臨床知見からの提言
全国の先生方より、消化器および皮膚領域における最新の診療状況を踏まえた上で、様々な視点から顆粒球吸着療法(GMA)の日常診療における活用方法や工夫、メリットや課題についてお話いただきます。
IBD:炎症性腸疾患、UC:潰瘍性大腸炎、CD:クローン病、PP:膿疱性乾癬、PsA:乾癬性関節炎(関節症性乾癬)
※先生のご所属先および役職、治療指針等は掲載時点の情報です
土谷総合病院におけるIBD診療の実際
当院は、広島市の中心市街地に位置し、平和記念公園に隣接する394床(2024年6月現在)の急性期総合病院です。開業より腎疾患の治療に注力し、透析医療へ先駆的に取り組んできた歴史を持ち、現在は小児を含む循環器疾患に対して、不整脈のカテーテルアブレーション等をはじめとして豊富な診療実績を有しています。IBDに関しては、私の着任を契機として積極的に取り組みはじめ、徐々に患者数も増加し、2024年4月に炎症性腸疾患外来の設置に至りました。今では、地域医療連携による紹介患者さんも増えており、立地条件の良さから年齢や職業など幅広い背景のIBD患者さんが来院されています。
近年のIBD治療の進歩により、外科的介入の頻度は減少しましたが、それでも一定数は存在し、また、腸管外合併症も少なくないことから、治療成績およびQOL向上のために、円滑な多科連携は重要なポイントとなります。当院においても、外科はもとより整形外科や皮膚科と綿密な連携を図っており、カンファレンスも活用しながら、コンサルトを必要とする症例について一丸となって治療に臨んでいます。一方GMAは、私が着任するまで未導入でしたが、腎・血液浄化療法科の医師と臨床工学技士が導入に向けて積極的に取り組んでいただいたおかげで、2023年10月以降、ほぼ連日の施行が可能となり、現在は、IBD専門外来の曜日に施行人数を増やせるフレキシブルな体制も整備されています。IBDは、下痢などの腸管症状のみならず、体重減少や皮膚病変などの全身症状を伴うことも少なくないため、多科連携に加え、栄養士や看護師、臨床工学技士などによる多職種連携を推進させる意義はきわめて大きいと考えます。
現代のUC診療の実情と課題
従来、UC治療は5-アミノサリチル酸(5-ASA)製剤やステロイド注腸など炎症抑制が中心でしたが、2000年以降、生物学的製剤(Bio)やJAK阻害薬などの治療選択肢が大幅に増加し、免疫抑制を主体とする治療が一般化しました。このような状況においても、5-ASA製剤やステロイドなど既存治療の重要性は変わることなく、治療指針に則って5-ASA製剤の十分量投与による初期治療を行い、それでも症状が残存する場合にステロイドやGMAにより強化を図るステップアップ療法が基本的な治療戦略と考えます。
このようにUC治療のベースとなる5-ASA製剤に対して、近年、アレルギーや不耐を呈する症例が増加しています1)。その背景には、日本人全体としてアレルギー症状が発現しやすくなっている可能性も考えられ、実際に厚労省の統計では、アレルギー疾患により医療機関を受診する患者数は増加傾向を示しています2)。その他にも、現代UC治療において留意する点として、小児の成長障害や挙児希望、高齢者はポリファーマシーや癌をはじめとした併存症など、多様な患者背景への考慮が強く求められています。
当院は循環器系に注力する施設であることから、脳心血管病併存の高齢UC患者さんを紹介されるケースも少なくありません。抗血小板剤を服用中にUCが高齢発症したケースでは、生命予後に関わる抗血栓療法の中止が困難な状況下で、腸管からの出血をコントロールする必要があるため、必然的に治療が難渋化します。また、このような脳心血管病を併存するIBD治療を考える際、例えばJAK阻害薬における心血管イベント※など、各薬剤で報告されている副作用やリスクを考慮しなければならないため、より慎重な治療薬の選択が求められます。(※ 循環器系危険因子を有する50歳以上の関節リウマチ患者における報告3))
その他にも、高齢UC患者さんでは、担癌および癌の既往歴や腎機能低下などを認めやすいため、それぞれTNF-α抗体製剤やカルシニューリン阻害剤の投与には十分な注意が求められます。このように、IBD治療では腸管の炎症のみを診療するのではなく、患者さんの全身状態について十分把握し、長期的なQOLを見据えた治療が望まれていると考えます。
UC治療におけるGMAの位置付け、役割
UC治療は長期に及ぶことから、患者さんの将来を見据え、安全面を考慮した治療選択が望まれます。GMAは、20年を超える臨床経験を有しており、非薬物療法である点から長期的な安全性を推測すると、特に小児や青年期の患者さんにとって、期待できる選択肢の一つと捉えています4)。このため、治療方針の共同意思決定(SDM)の際、ステロイドをはじめとした薬物療法の効果と安全性の説明に加え、長期的な視点からGMAの安全性についても患者さんへ提示し、共に治療方針を策定しています。
私の経験ですが、2010年以前はUCの5-ASA製剤を除けば治療選択肢に乏しく、ステロイドが中心的な役割を果たす状況下で、若い患者さんにはGMAを勧める場合が一般的でした。当時、学生であったUC患者さんとのSDMの際に、患者さんのご家族からの希望もありGMAが選択され、穿刺を我慢しながら治療を確実に継続し、立派な社会人に成長されたケースを経験しました。現在は母親となって、当時の親の思いを知り、私にも感謝を伝えていただいたことは医師冥利に尽きる出来事となりました。
この症例では、ステロイドによる容姿変化など副作用発現の回避に注力しましたが、GMAにはステロイド総投与量の減少が報告されており5)、ステロイド使用時にはGMAの併用を選択肢の一つと考えています。従って、5-ASA製剤による改善が乏しい若年層の「慢性持続型で中等症の難治性UC」に対して、GMAはステロイド導入前の選択肢、あるいはステロイドとの併用が位置付けとして期待できるのではないでしょうか。
私が担当してきた11~19歳の平均CAI(Clinical Activity Index)スコアが14.1であったステロイドナイーブのUC 34例におけるレトロスペクティブ解析6)の結果、5-ASA製剤による初期治療に対し効果不十分であった22例にGMAを導入していました【図】。GMAは、導入週に2回施行(初回および2回目は週2回のペース)、その後は最大11回まで週1回のペースで行い、5回終了時点で中間効果判定を実施しました。その際、CAIが5点以上低下した12例ではGMA単独治療を継続し、治療開始から12週目には平均CAIが2.1点まで改善されていました。一方、中間効果判定においてCAIが上昇もしくは5点以上が継続した場合、体重1kgあたり0.5~1.0mg/日のステロイドを併用したところ、治療開始から12週目には全例が臨床的寛解に至り、投与3カ月以内にステロイドフリーとなりました。なお、これら大部分の症例で粘膜治癒が認められています。
GMAのステロイドナイーブ例(慢性持続型で中等症の難治性UC)に対する効果は、若年層のみならず、幅広い年齢層において期待できます。私の経験では、平均年齢44.7歳の45例におけるGMAの寛解率はステロイドナイーブ例が84.6%、ステロイド依存例が57.9%でした7)。このように、難治性中等症のUCに対して、GMAは効果が期待されますが、深掘れ潰瘍などを認める重症例に対しては、GMA単独での奏効は難しく、薬物療法との併用が望まれます。
その他にも、循環器疾患や癌の既往歴などからJAK阻害薬や生物学的製剤の投与が躊躇される場合の治療強化としてGMAの併用は有用と考えています。また、PARTICULAR study8)では、高齢者などスペシャルシチュエーションのIBD患者さんに対するGMAの安全性および有効性が示されており、GMAの役割が期待されます。
最後に、GMA施行中の患者さんの中には『お腹がじわりと暖かくなる』や『お腹が良くなってくるのが分かる』と感じる方が散見されます。カラム内部に単球や顆粒球が吸着した後、腸管における微細な変化を鋭敏に感じ取っている可能性や、私を含め積極的に話しかける医療スタッフの存在が安心感を与えている可能性も考えられます。GMA治療中の温感について、治療効果の予測因子としての検討も行われており9)、今後の更なる治療成績向上のために、知見の集積が望まれます。
1) Hiraoka, S. et al.:J Gastroenterol Hepatol. 2021;36(1):137-143.
2) 厚生労働省:アレルギー疾患の現状等 平成28年2月3日, https://www.mhlw.go.jp/file/05-Shingikai-10905100-Kenkoukyoku-Ganshippeitaisakuka/0000111693.pdf (2024年6月現在)
3) Ytterberg, SR. et al.:N Engl J Med. 2022;386(4):316-326.
4) Tanaka, T. et al.:Expert Rev Gastroenterol Hepatol. 2017;11(8):749-758.
5) 下山孝ほか:日本アフェレシス学会雑誌 1999;18(1):117-131.
(利益相反:本研究はJIMROの資金提供を受けて行われた。)
6) Tanaka, T.:Cureus. 2023;15(11):e48913.
7) Tanaka, T. et al.:Dig Liver Dis. 2008;40(9):731-736.
8) Motoya, S. et al.:BMC Gastroenterol. 2019;19(1):196.
(利益相反:本研究は一部JIMROの資金提供を受けて行われた。著者の一部はJIMROの社員である。)
9) 飯塚 政弘:厚生労働科学研究費補助金(難治性疾患政策研究事業) 難治性炎症性腸管障害に関する調査研究 分担研究報告書, 令和3年度:217.