GMAのこれまでとこれから:GMAのクリニカルパール探求
アダカラムインタビュー記事シリーズ
GMA 20年をこえる臨床知見からの提言
全国の先生方より、消化器および皮膚領域における最新の診療状況を踏まえた上で、様々な視点から顆粒球吸着療法(GMA)の日常診療における活用方法や工夫、メリットや課題についてお話いただきます。
IBD:炎症性腸疾患、UC:潰瘍性大腸炎、CD:クローン病、PP:膿疱性乾癬、PsA:乾癬性関節炎(関節症性乾癬)
※先生のご所属先および役職、治療指針等は掲載時点の情報です
関西医科大学における乾癬診療の実際
当センターにおいて、心血管疾患やメタボリック症候群の対策に注力する背景には、乾癬患者さんは、糖尿病や高脂血症、高血圧の罹患率が非乾癬患者さんよりも有意に高く1) 、死因の第一位が心血管疾患である点があげられます2) 。実際に、当院を受診された乾癬患者88名の調査では、冠動脈CT造影(CCTA)の異常所見を44.3%に認め、要治療者は全体の15.9%に及んでいました3) 。そして、CCTAの異常所見は、足関節上腕血圧比(ABI)が0.7未満の場合、0.7以上に比べ有意に上昇していたことから、ABI<0.7が乾癬患者における心血管疾患のスクリーニングに適している可能性が示唆されました。ABIの測定は比較的簡便であるため、医療経済的視点も含め、今後の更なる知見の集積が期待されます。
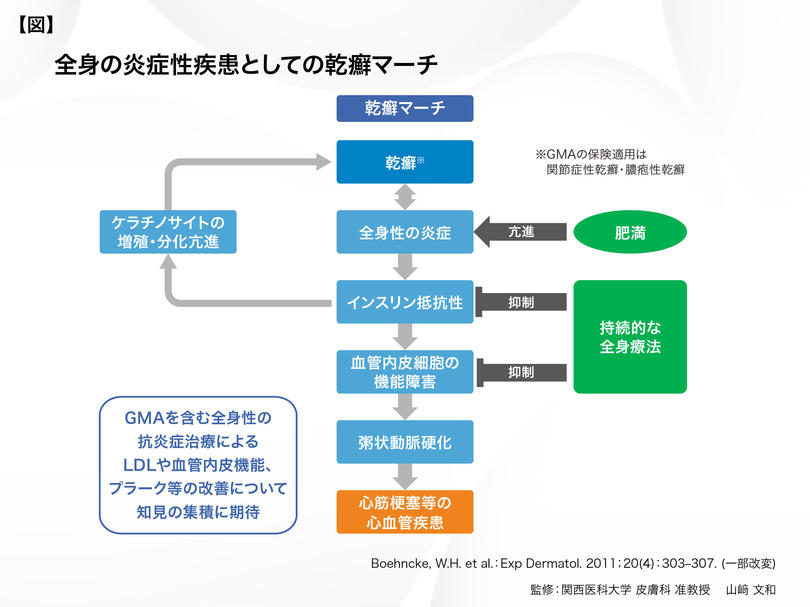
現在、乾癬は全身の炎症性疾患と捉えられており、冠動脈をはじめとした心血管病変の発現に至る現象は、"乾癬マーチ"と称され【図 】、大きな注目を集めています。推測されている機序としては、まず乾癬による全身性の炎症が、肥満とも相まってインスリン抵抗性を惹起します。インスリン抵抗性は、ケラチノサイトの増殖と分化を促し、乾癬の悪化を招くと同時に、血管内皮細胞の機能障害も導きます。すると動脈内膜に単球が侵入しやすくなり、LDLを貪食しながらプラークを形成する粥状動脈硬化(アテローム性動脈硬化)に至ります。これにより血管が狭くなって心筋梗塞など心血管疾患のリスクが上昇すると考えられています。
当センターでは、乾癬マーチの進行を抑制するために栄養指導を重要視しており、個々の患者さんの性格に適した栄養介入や、間歇スキャン式持続血糖測定器を用いたモニタリングなどについて臨床知見の集積を進めています。乾癬マーチの進行抑制においては、このような栄養をはじめとした生活習慣の改善に加え、全身性の炎症を確実にコントロールする点も重要となります。私たちは、器質的な冠病変を認め、血圧以外には異常がない乾癬患者さんに対して、抗IL-17A抗体製剤を2年間投与し追跡調査を行ったところ、スタチン製剤が未投与であったにも関わらず、CCTAにより冠病変の形態変化が示されたケースを報告しています4) 。
この症例報告は、2019年に行いましたが、その後も同様の報告が続き、当センターでも機序の異なる生物学的製剤(Bio)によって冠動脈の形態変化を認めていることから、乾癬マーチの抑制に向けて全身性の炎症コントロールの意義は大きいと考えています。今後、GMAを含む全身性の抗炎症治療による脂質代謝や血管内皮機能、さらに冠病変や生命予後への効果についてもエビデンスの構築に期待しています。
関西医科大学のPsA診療における非薬物療法の意義
光線療法に関しては、中波長紫外線(UVB)から有害な波長を除去し、治療効果の高い波長を照射可能な"ナローバンドUVB療法"が2000年代に開発されたことを契機に、340~400nmの長波長紫外線(UVA)を用いる"UVA1療法"、発疹のみにナローバンドUVBを照射する"ターゲット型エキシマランプ"などが続々と臨床の場に登場しました。これら光線療法によって、治療成績の向上や発癌などの安全性が改善され、欧米や日本において数多くのエビデンスが蓄積されました。
実臨床において、光線療法は非薬物療法として安全性に優れることから、高齢者や担癌患者さんに適しており、Bio導入の前に光線療法のみでコントロールできれば治療選択肢の一つとして意義が大きいと考えます。また、光線療法は外用薬との親和性が高く、両者の併用により相加的な効果も期待されます。光線療法は、他治療とも組み合わせることが可能であり、すそ野が広くフレキシビリティに優れた治療と捉えています。
関西医科大学におけるGMAの位置付け、活用法 5) において報告されています。したがってGMAは、光線療法と同様に安全性への配慮が必要なPsA患者さんへ用いることが可能な治療と考えます。特に、高齢者や担癌患者さん、妊娠中や妊娠希望の患者さんに対して、選択肢の一つとして考慮される治療ではないでしょうか。
当センターにおけるGMAの施行例としては、Bioを使用していても軽度から中等度の痛みが残存するようなPsA患者さんに対して、痛みの改善を期待してGMAを併用することで治療強化を図っています。PsA患者さんの中には、腎機能や肝機能、消化管粘膜傷害、薬物相互作用などの観点から非ステロイド性抗炎症薬(NSAIDs)や合成抗リウマチ薬(sDMARDs)の投与を回避したい場合も少なくありません。このように薬物療法が使用しにくいシチュエーションにおいて、非薬物療法であるGMAにより臨床症状が改善されれば、その意義は大きいと推察されます。PsAに対するGMAの治験結果6) およびこれまでの使用経験より、GMAはPsAの疼痛改善に寄与すると考えられ、今後の自覚症状改善に着目した知見の集積に期待しています。
PsA治療における課題として、Bioの効果減弱(LOR)が一定頻度で発現してしまう点が挙げられます。LORでは、Bioに対する中和抗体産生による有効血中濃度の低下が一因となりますが、抗TNFα抗体製剤の場合、メトトレキサート(MTX)の併用による中和抗体の産生抑制が報告されています7) 。IBDにおける検討ではあるものの、抗TNFα抗体製剤とGMAの併用による血中の中和抗体およびIL-6濃度の低下が報告されており8) 、PsAにおいても同様の現象を示す可能性も考えられます。
このように、GMAは抗TNFα抗体製剤との併用において、中和抗体の面からも効果を補う役割が期待されますが、他のBioに関してもGMAの作用機序から鑑みて、併用した際に作用を阻害する可能性は低く、安全性への影響も小さいことが類推されます。今後、PsA治療におけるGMAと様々なBioとの併用に関して、効果と安全性の双方から知見の集積が望まれます。
1) Takahashi, H. et al.:J Dermatol. 2012;39(3):212-218.